Рівняння стану ідеального газу (рівняння Менделєєва-Клапейрона):
\(P\) — тиск;
\(V\) — об'єм;
\(n\) — кількість речовини;
— стала Больцмана;
\(T\) — температура.
Рівняння Клапейрона:
або
Ізопроцес — це процес, у ході якого один із макроскопічних параметрів даного газу деякої маси залишається незмінним. Оскільки стан газу визначеної маси характеризується трьома макроскопічними параметрами, то можливих ізопроцесів стільки-ж: процес за незмінного тиску, незмінного об'єму та незмінної температури.
Зверни увагу!
Кожному ізопроцесу відповідає свій закон:
| Ізотермічний процес — процес змінювання даного газу деякої маси, що відбувається за незмінної температури. |
Закон Бойля-Маріотта:
|
| Ізобарний процес — процес змінювання даного газу деякої маси, що відбувається за незмінного тиску. |
Закон Гей-Люссака:
|
| Ізохорний процес — процес змінювання даного газу деякої маси, що відбувається за незмінного об'єму. |
Закон Шарля:
|
Кожний ізопроцес можна зобразити на графіку:
| Система координат: | PV | PT | VT |
| Ізотермічний процес | 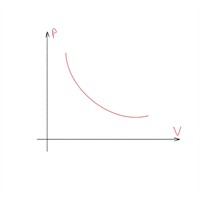 |
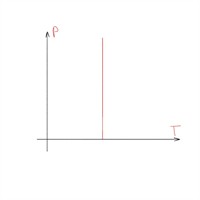 |
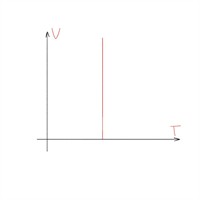 |
| Ізохорний процес | 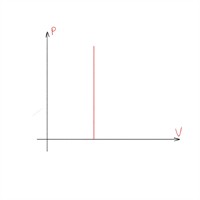 |
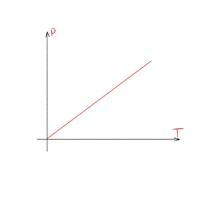 |
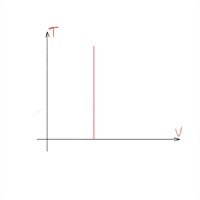 |
| Ізобарний процес | 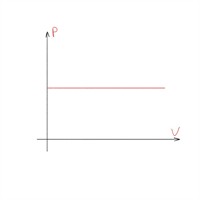 |
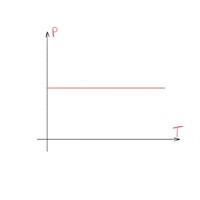 |
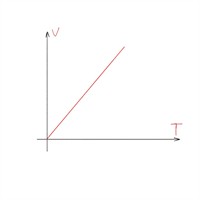 |