Розділ хімії, який вивчає швидкість і механізми протікання хімічних реакцій — хімічна кінетика.
Швидкість хімічної реакції — це зміна концентрації реагуючих речовин за одиницю часу.
Для реакції, що протікає за рівнянням:
швидкість реакції можна розрахувати за зміною концентрації одного з реагуючих речовин, наприклад, речовини \(A\).
Якщо у момент часу концентрація речовини \(A\) дорівнює , а у момент часу концентрація речовини \(A\) зменшилася, і стала рівною , то швидкість можна визначити як зміну концентрації речовини \(A\) за промежок часу:
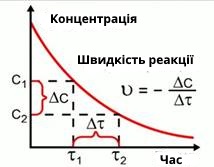
Швидкість є позитивною величиною, а концентрація реагуючих речовин зменшується.
Тому у формулі швидкості в загальному вигляді використовують знак плюс-мінус.
Швидкість хімічної реакції залежить від:
природи реагуючих речовин;
концентрації реагуючих речовин;
температури;
наявності каталізатору.